Page 42 - 《涂层与防护》2020年第2期
P. 42
赵鹏飞,等:2-苯基咪唑啉/多元羧酸化学消光体系反应速度差定量研究
过把各自的动力学参数代入方程(7)可得到各反应体
2.2 反应速度差与光泽的关系
系的动力学方程。 这里假设固化温度为 200 ℃ (T=
473.15 K),反应刚开始时,固化度 α=0,此时的反应速 将 B31 与多元酸进行复配, 加入环氧体系中,根
度 dα/dt 即为固化反应的初始速度,单位为%/s。 据表 3 配方进行制粉并喷涂固化,得到具有不同光泽
表 5 各固化体系反应动力学参数值及初始固化速度
-1
A (s ) E (kJ/mol) n dα/dt (α=0, %/s)
环氧/B31 2.43×10 6 54.30 0.92 2.461
环氧/PMA 1.16×10 11 104.66 0.94 0.325
环氧/PMDA 3.36×10 6 63.61 0.92 0.319
环氧/BTA 4.81×10 15 143.96 0.95 0.614
环氧/TMAH 5.48×10 12 115.75 0.94 0.911
环氧/TMAC 1.02×10 11 102.91 0.94 0.441
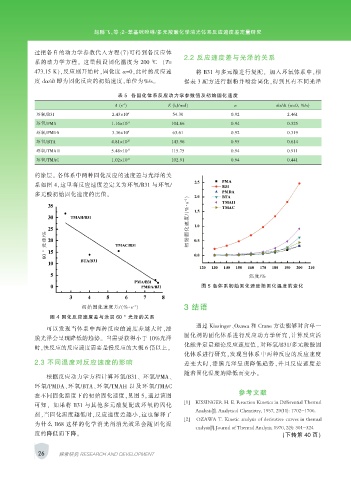
的涂层。 各体系中两种固化反应的速度差与光泽的关
系如图 4,这里将反应速度差定义为环氧/B31 与环氧/
多元酸初始固化速度的比值。
初始固化速度/(% · s -1 )
光泽/%
°
60
温度/%
图 5 各体系初始固化速度随固化温度的变化
-1
初始固化速度差/(% · s ) 3 结语
图 4 固化反应速度差与涂层 60 ° 光泽的关系
通过 Kissinger、Ozawa 和 Crane 方法能够对含单一
可以发现当体系中两种反应的速度差越大时,漆
固化剂的固化体系进行反应动力学研究,计算反应活
膜光泽会呈现降低的趋势。 当需要获得小于 10%光泽
化能并定量理论反应速度值。 对环氧/B31/多元羧酸固
时,快反应的反应速度需要是慢反应的大概 6 倍以上。
化体系进行研究,发现当体系中两种反应的反应速度
2.3 不同温度对反应速度的影响 差变大时,漆膜光泽呈现降低趋势,并且反应速度差
随着固化温度的降低而变小。
根据反应动力学方程计算环氧/B31、 环氧/PMA、
环 氧/PMDA、环 氧/BTA、环 氧/TMAH 以 及 环 氧/TMAC
参考文献
在不同固化温度下的初始固化速度,见图 5。通过该图
[1] KISSINGER H. E. Reaction Kinetics in Differential Thermal
可知, 如果将 B31 与其他多元酸复配成环氧的固化
Analysis[J]. Analytical Chemistry, 1957, 29(11): 1702-1706.
剂,当固化温度越低时,反应速度差越小,这也解释了
[2] OZAWA T. Kinetic analysis of derivative curves in thermal
为什么 B68 这样的化学消光剂消光效果会随固化温
analysis[J]. Journal of Thermal Analysis, 1970, 2(3): 301-324.
度的降低而下降。 (下转第 40 页)
26 探索研究 RESEARCH AND DEVELOPMENT